تتكون الروابط التساهمية عندما - تتكون الروابط التساهمية عندما

Recent Posts
- مريول نوري طريق الدمام
- تشكن ات
- قناة الكويت الرياضية
- من الوقفات في التايكوندو
- المستشفى العسكري بوادي الدواسر
- اضافه مواد ضاره الى التربه او الماء او الهواء
- فعاليات يوم التأسيس الشرقيه
- رقم اس تي سي باي
- كحل ذا بالم
- اجمل دعاء إلى الله
- شيله اسمحلي اشوفك
- كم باقي على الصيف العد التنازلي
- طلولي
- وهو الذي ينزل الغيث من بعد ما قنطوا وينشر رحمته وهو الولي الحميد
- افلام مصريه
- تحتوي أجسام الحيوانات الفقارية على العمود الفقري
- المقصود بالظلم هو
- شانجان cs75 2022
- مطعم البيت بيتك ابها
- برادايز لقطف الفواكه
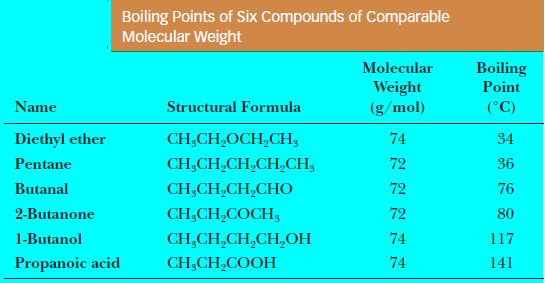
تتكون الروابط التساهمية عندما؟
الرابطة التساهمية القطبية يوجد هذا النوع من الرابطة التساهمية حيث تحدث المشاركة غير المتكافئة للإلكترونات بسبب الفرق في الكهربية لدمج الذرات.
تحتوي جزيئات الأمونيا على ذرة واحدة من النيتروجين بها خمسة إلكترونات تكافؤ.
الرابطة التساهمية
ومثال للرابطة الثنائية في حمض النيتروس بين N و O , ومثال للرابطة الثلاثية سيانيد الهيدروجين بين C و H.
مثال على الروابط الأيونية تترابط أيونات الصوديوم الموجبة، مع أيونات الكلوريد السالبة، من خلال فقد الصوديوم لإلكترون واحد، وإعطائه للكلور، وذلك لتكوين كلوريد الصوديوم، أو ما يُسمى بملح الطعام.
- Related articles
2022 encompassinc.co